Unidad de investigación clínica
Servicios
Qué estudios se pueden realizar?
- Ensayos clínicos sin un objetivo terapéutico en voluntarios sanos:
- Estudios farmacocinéticos y metabolismo (incluyendo los ensayos de bioequivalencia, tolerabilidad, primera administración en humanos dosis única o dosis múltiple)
- Efectos farmacodinámicos: efectos subjetivos, seguridad cardiovascular.
- Efectos en la conducta, evaluación de estrés.
- Ensayos clínicos fase I y fase II de eficacia y tolerabilidad.
- Ensayos clínicos fase I en poblaciones especiales (Pediatría, ancianos, síndrome de Down o del X-Frágil, consumidores de sustancias tóxicas o adictivas)
- Estudios de interacciones fármaco-fármaco
- Ensayos clínicos de intervención nutricional.
- Beneficios de la nutrición para la salud en el rendimiento cognitivo
- Estudios de interacción fármaco-alimento
- Colaboraciones en ensayos clínicos de fase II-IV: visitas de selección, extracciones de muestras, biopsias, cuestionarios.
- Estudios de medición de función renal.
- Estudios de excreción en el marco del control del dopaje
- Determinación e identificación de fármacos y metabolitos, en sangre, orina, cabello, saliva y otras matrices biológicas. Estudios metabolómicos dirigidos.
Equipos
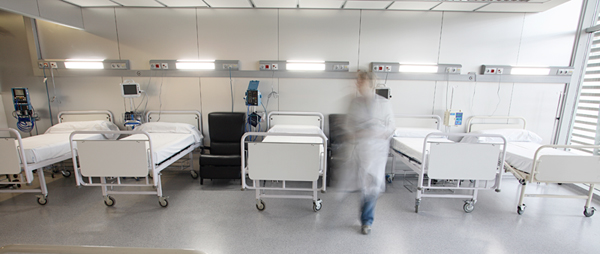
La Unidad de Investigación Clínica (URC) dispone de unas instalaciones con capacidad para 12 voluntarios en la zona de ingreso y tres dispensarios para realizar las visitas de selección y las evaluaciones ambulatorias.
Alta capacidad de reclutamiento, base de datos de más de 500 voluntarios.
Política de calidad: La Unidad dispone de Procedimientos Normalizados de Trabajo con el fin de garantizar los derechos y seguridad de los pacientes y la calidad de los datos obtenido de los estudios, dando cumplimiento a las Normas de Buena Práctica Clínica y normativas vigentes en materia de Ensayos clínicos.
La Unidad es acreditada periódicamente por la Generalitat de Catalunya y su actividad es auditada por la Unidad de Calidad del IMIM.
El equipo de profesionales que la integra:
- es multidisciplinar (farmacólogo(a)s clínico(a)s, enfermeras, farmacéutico(a)s, neuropsicólogo(a)s…) especializado en actividades de investigación clínica.
- han colaborado en la puesta en marcha y desarrollo de ensayos clínicos promovidos o copromovidos por diferentes grupos de investigación en varias áreas terapéuticas, por la industria farmacéutica y de la alimentación.
trabajan en estrecha colaboración con el Grupo Farmacología Integrada y Neurociencia de Sistemas y la Agencia Mundial Antidopaje. - Están vinculados con el Parc de Salut el Mar (Hospital del Mar) y las Universidades Pompeu Fabra y Autónoma de Barcelona.